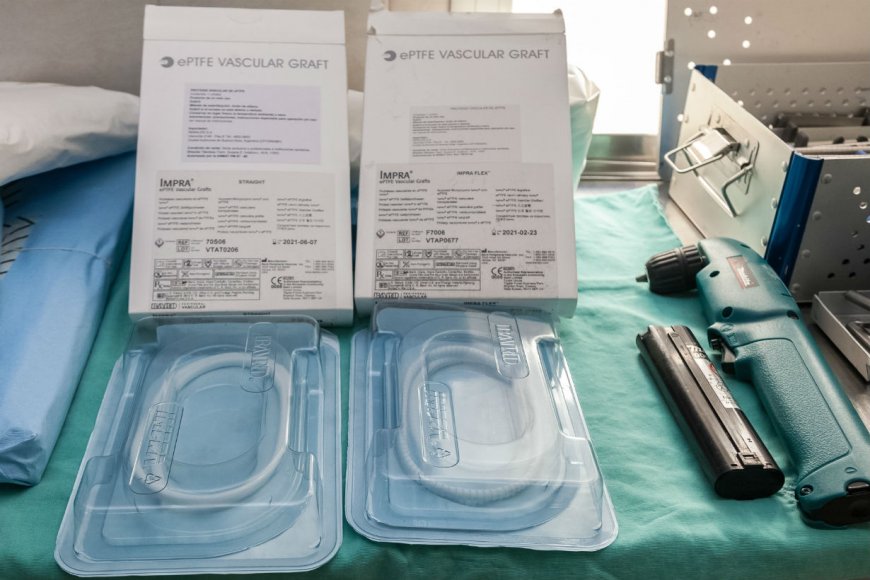
En una primera etapa la aplicación, alcanzará a cardiodesfibriladores/cardioversores, estimuladores eléctricos para la audición en la cóclea, lentes intraoculares, marcapasos cardíacos, endoprótesis (stent) vasculares coronarios, prótesis de mama internas, de cadera y de columna.
“Con esta medida, buscamos contrarrestar el impacto negativo que la distribución de productos médicos ilegítimos representa para la salud de los pacientes y el sistema sanitario, siempre orientados a recuperar la rectoría del Ministerio de Salud en el dictado de normas que permitan mejorar la calidad de los servicios”, resaltó la titular de la cartera sanitaria, Sonia Velázquez, y en ese sentido precisó que “esta instancia permitirá el seguimiento, a través de toda la cadena de distribución, con la identificación, individual y unívoca, de cada unidad de las especialidades medicinales”.
Por su parte, la titular del Departamento Integral del Medicamento, Cristina Collino, explicó que la disposición 727/13 de la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (Anmat) establece la condición de venta de los productos mencionados. “La trazabilidad es poder realizar el seguimiento desde el laboratorio elaborador, pasando por un distribuidor habilitado y que llegue a un establecimiento en donde profesionales, farmacéuticos y médicos de los servicios de Traumatología o Cardiología, verifiquen que ese producto es legítimo y que llegó en óptimas condiciones”, dio a conocer.
Para garantizar que llegue al paciente un producto médico seguro, los efectores públicos y privados que los implanten deberán inscribirse en la Anmat y obtener un código de alta en el sistema. Además, cada uno de los insumos ostenta una tarjeta de implante con un número que certifica que viene de un laboratorio habilitado, pasó por una cadena legal de comercialización y reúne las características de seguridad.